乐伐替尼,改进型新药是在原有药物根底上停止改良,有一定临床根底,大局部产品不需求停止完好临床实验,在市场竞争中具有较大优势。改进型新药可请求打破性医治药物,享用国度政策红利。在全球新药研发失败率越来越高,开发新靶点越来越难的状况下,关于无法承当创新转型的仿制药企业,改进型新药或许是一个最佳选择。
改进型新药概略
2016年化学药品新注册分类重新定义了新药及仿制药的概念,新药强调全球新,包括创新药和改进型新药。改进型新药是对已上市药品的改良,强调“优效性”,具有高成功率、高报答、低风险、生命周期长等优势,已成为全球新药研发的主流。在我国带量推销和鼓舞药品创新等政策的影响下,改进型新药将继续被市场看好,高销售费用向高研发投入的转变将成必定。
2010年以来,我国药企在改剂型方面,偏好于将普通片改胶囊、改分散片、改缓释片,多半是为改而改,缺乏思索其临床价值。这些产品,尤其是缓释制剂,曾经成为仿制药质量和疗效分歧性评价中的“三改”种类。
改进型新药分类和申报
为鼓舞新药创制,严厉审评审批,进步药质量量,促进产业晋级。原CFDA于2016年3月发布了《化学药品注册分类变革任务方案》,对化学药品注册分类停止变革,重新定义“新药”,并进一步分为1类新药和2类新药。
表1 2类新药分类包括情形及案例
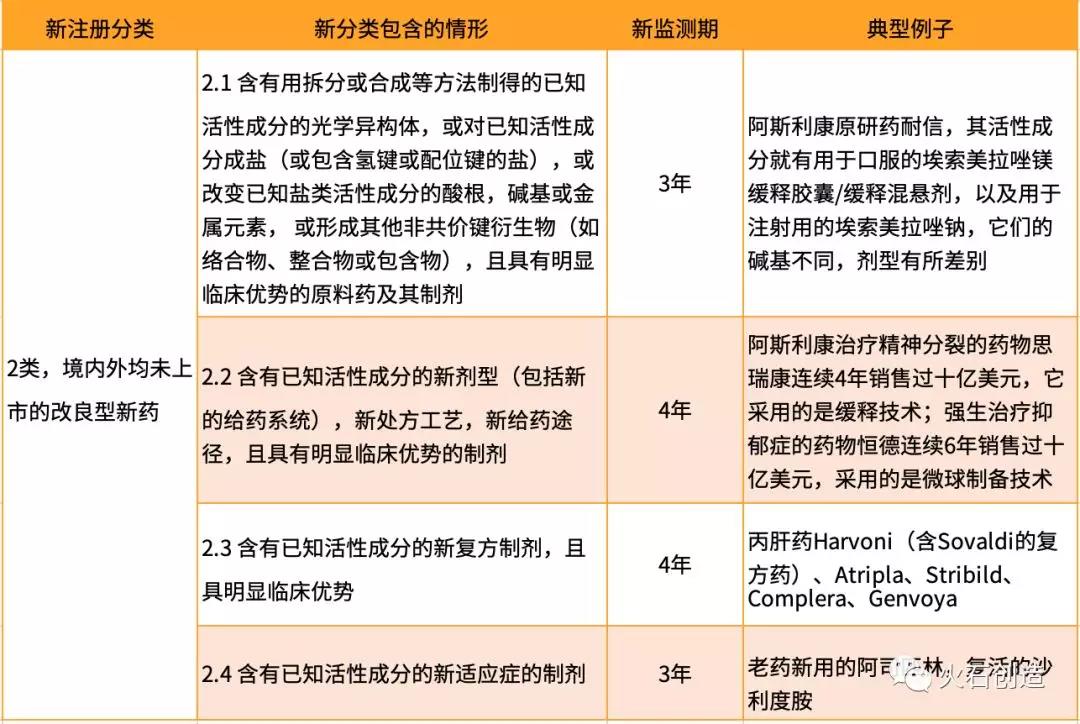
新2类强调“优效性”,指在已知活性成份的根底上,对其构造、剂型、处方工艺、给药途径、顺应症等停止优化,且具有分明临床优势,且境内外均未上市的改进型新药。
2类新药按新药途径申报包括4类:构造改进、剂型改进、新复方制剂和新顺应症。依据食品药品监管总局发布的《化学药品新注册分类申报材料要求》,1、2类新药采用同一套注册文件零碎,2类新药需提交原研药品信息,不需求填写化学药品IND请求药学研讨信息汇总表,但在《立标题的与根据》中,需求专门阐明拟处理的成绩和支持其具有分明临床优势的证据。
因而,四类改进型新药需经过不同方式对原研药物停止改进,以完成更优的临床效果。可以说,新2类化药注册要求根本堵死了以前盛行的低程度改剂型、给药途径、改酸根碱基成酯类“新药”的路。
改进型新药优势
临床需求方面优势
改进型新药具有分明的临床优势。改进型新药是对已上市药品的晋级改进,强调“优效性”,相较于被改进的药品,具有加强药效、降低反作用、进步患者的服药依从性等分明的临床优势。
1. 有助于进步药物效果。例如亮丙瑞林微球构造使药物活性成分不易被酶降解,改善药物波动性,明显进步药物效果。
2. 增加用药次数,加强患者顺应性。例如利培酮代谢产物前药超长效制剂3个月肌注一次,一年只需注射4次,与每日给药的惯例剂型相比,大大增加了给药次数,加强了患者的用药依从性。
3. 降低反作用,改善平安性。例如紫杉醇白蛋白纳米粒采用纳米粒技术,将药物结合于人血白蛋白构成直径为130 nm的颗粒,过敏反响发作率极低,血液毒性、消化道毒性及神经毒性均低于紫杉醇注射液及紫杉醇脂质体。
图1 改进型新药具有分明的临床优势
药物研发方面优势
在药物经济学方面,改进型新药具有低风险、低投入、长生命周期、高报答的优势。
1. 与新分子实体相比,改进型新药的研发风险较低,投入本钱低。
在研发风险方面,改进型新药的研发成功率约是新分子实体的3.6倍,研发风险分明低于新分子实体。
在资金、工夫投入方面,开发一个新分子实体药需求展开少量临床前研讨和临床研讨证明药物平安无效,一个新药的均匀研发费用达12亿美元,历时10~15年,而改进型新药可以参考曾经同意的药物或曾经宣布的文献,防止少量反复实验,大大增加研发费用和工夫,以新型制剂为例,均匀耗资只需0.5亿美元,历时仅3~4年。
2. 与仿制药相比,改进型新药技术或专利壁垒高,生命周期长,报答率高。
改进型新药与仿制药相比无论是构造改进、剂型改进、新复方制剂或许新顺应症,都有一定技术或专利壁垒,如脂质体、微球、纳米粒等工艺复杂以及BE难度大或需求临床验证。但是改进型新药相较仿制药有3~4年的监测期,生命周期分明拉长,报答率也明显提升。
改进型新药特征剖析
《化学药品注册分类变革任务方案》经过对创新药、改进型新药、仿制药停止差别化分类,施行更为精准高效的监管,以完成合理分配审批资源的迷信化管理。在政策中设立改进型新药,既可以防止不用要的低程度反复,又能完成针对创新研发的进一步细分,召唤企业关注已上市药品的优化改造。
在政策指引下,针对改进型新药展开的研讨逐步添加,后续的产品申报数量也在不时上升。只是,国际暂时还未出台对改进型新药的特殊监管渠道,配套的技术指点准绳和标准尚在探究论证阶段,对产品研发及评价带来一定的难度。从国际经历来看,美国新药请求的505(b) (2)途径比拟契合我国改进型新药政策的设计理念。
美国 505(b)(2) 现状
疾速崛起,成为美国新药市场主力
505(b)(2)请求获批产品数量不时攀升,上市后销售额有目共睹。近10年美国经过505(b)(2)请求获批的产品疾速添加,2017年环比增长40%,2018年请求获批的产品达75个,505(b)(2)途径申报的新药渐成研发主力,改进新药已成药研大势。
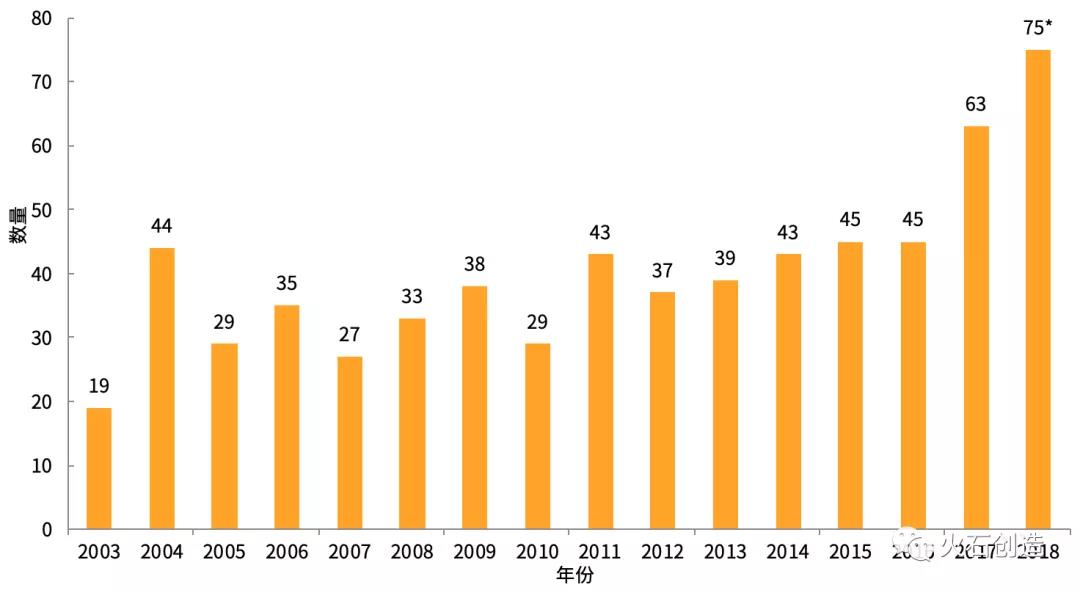
图2 2003—2018年美国505(b)(2)途径获批新药渐成主力
改进型新药上市后对普通剂型疾速替代。改进型新药上市后对普通剂型疾速替代,销售大约4~5年到达绝对波动,波动后创新制剂产品销售额占全体比例超越70%。
我国改进型新药现状
2类新药蒸蒸日上
类型散布
化药新注册分类施行已有3年半的工夫,依据CDE注册申报数据,共发布改进型新药受理号317个,其中2.4类受理号最多,有162个,占51% ;其次是 2.2 类,见图3。
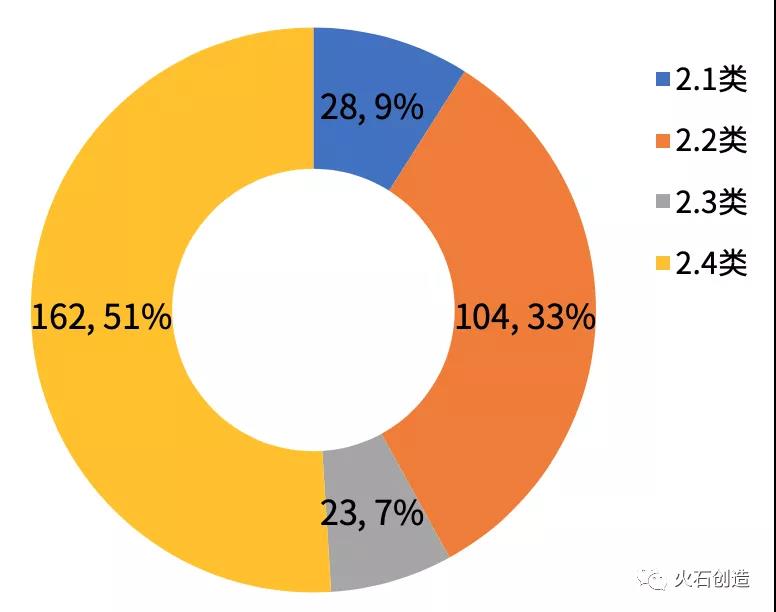
图3 我国CDE注册申报的改进型新药受理号类型散布
改进型新药的申报类型分为出口、新药和补充请求。317个改进型新药受理号中,2.1和2.2类以国际企业申报的新药为主,2.4类以国外企业申报的出口药为主,见图4。
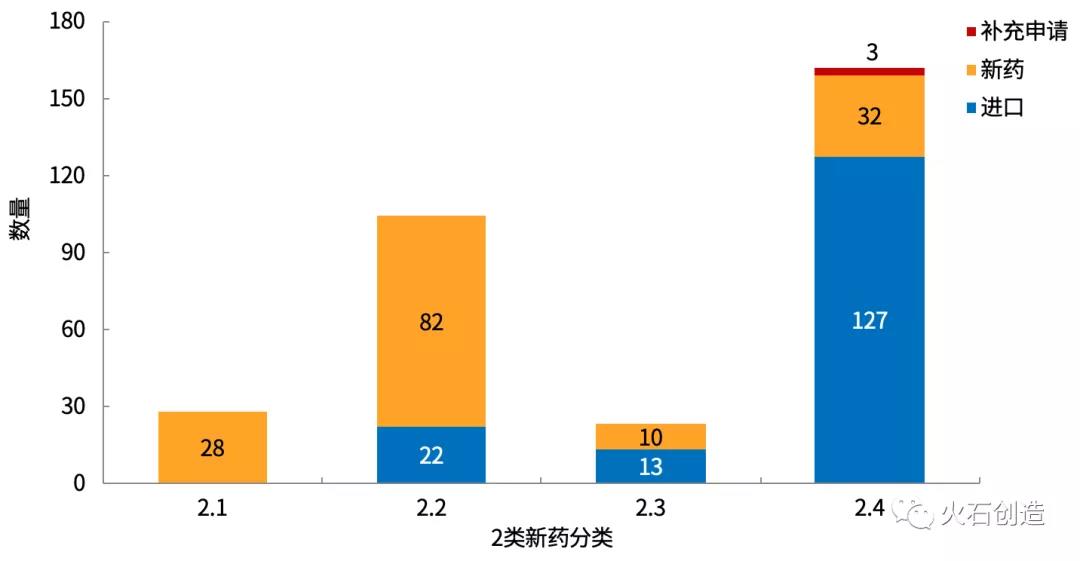
图4 不同改进型新药的申报类型散布状况
申报年份散布
我国2类尚处起步阶段,改进型新药的申报总数量出现逐年增长趋向。自2017年开端,2类新药申报数量呈现井喷式增长,其中2.2和2.4类申报数增长最为明显。见图5。
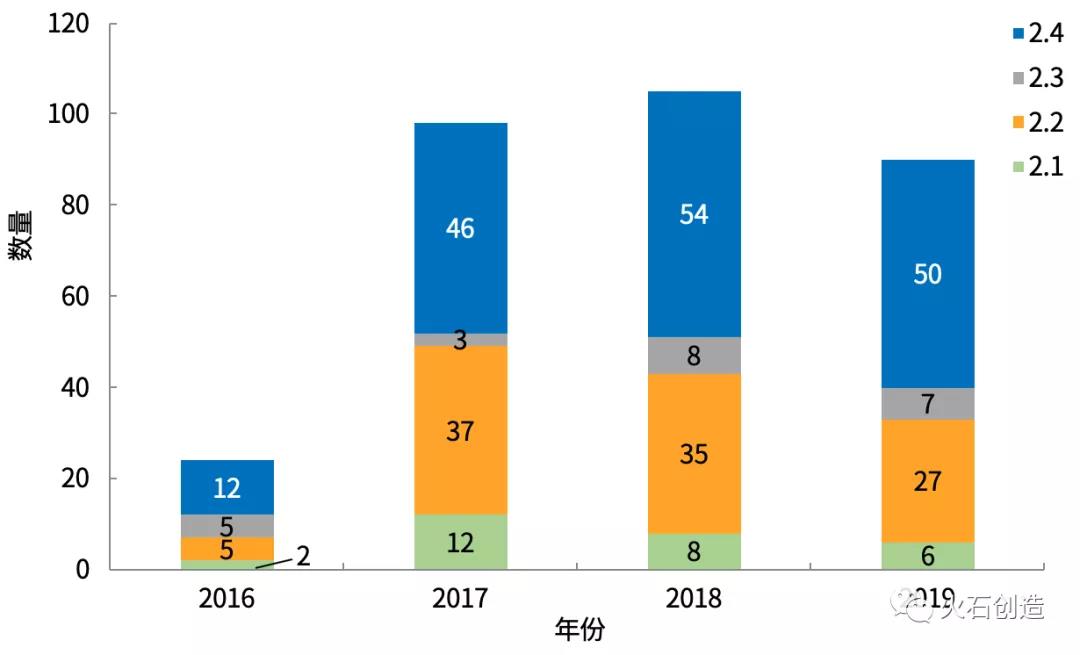
图5 2016年—2019年10月不同改进型新药申报数质变化状况
申报类别
国产改进型新药以2.2类为主,其次是2.4类新顺应症;而改盐基、改酸根碱基等小改动的2.1类的申报数量略有增加趋向。
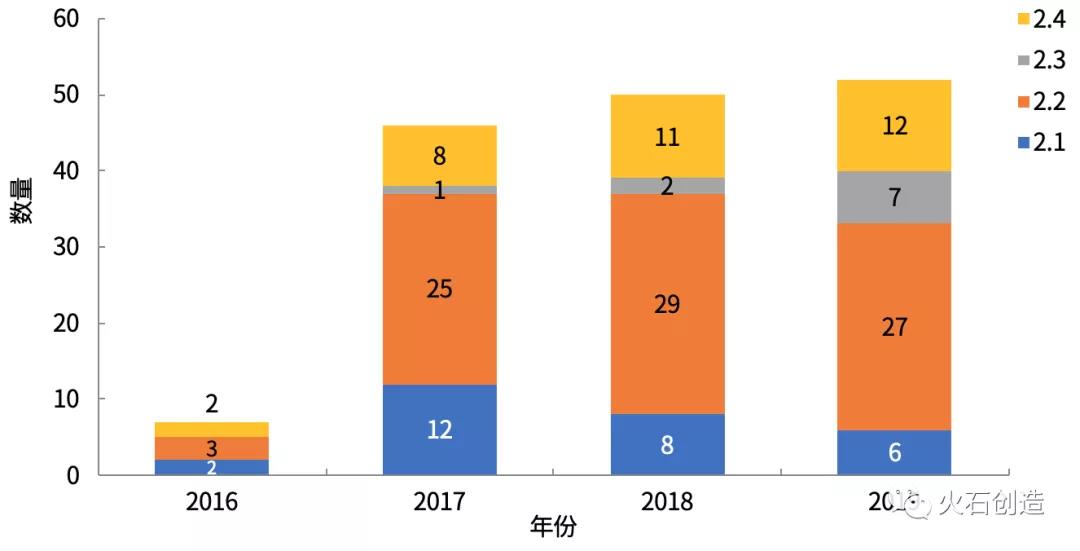
图6 2016—2019年10月国产改进型新药申报类别散布
中国改进型新药特征剖析
改剂型、新顺应症成为主流
2.2 类改进型新药次要针对新剂型、新工艺等改良,不改动药物的药理活性,次要经过剂型的优势表现产品的临床优势,这方面绝对比拟复杂,具有很明白的研发目的。同时很多改良不需求做大临床验证,由于活性成分未改动,只需求经过 BE 实验证明其药动学分歧即可。在本钱方面要小得多,这也契合我国目前企业的特点,所以申报数量呈逐年增多的趋向。
2.4 类改进型新药是新顺应症的申报,国外申报数量较多,就目前申报的药种类类来剖析,次要集中在肿瘤这一块,出口注册根本上被辉瑞、礼来、诺华、阿斯利康、勃林格殷格翰等这些跨国大公司占据。这次要是由于新出的抗肿瘤药物的顺应症只会有条件同意某一种肿瘤,随着研讨的愈加深化和医治工夫越来越长后,发现对其他肿瘤也无效,又会再次申报,故呈现这样的场面,国际的状况也是一样的。
2.1 类和 2.3 类研发热度较低
总览国际改进型申报数据发现,2.1 类和 2.3 类改进型新药申报较少,缘由有很多,但是次要是由于目前国际的药企普遍偏小,研发实力不强,只要极多数药企具有开发这类新药的才能,其次这两类新药必定会做大临床,以证明其疗效,研发工夫长、风险绝对较大。
三大要素驱动改进型新药行业疾速增长
需求端
慢病患者数量继续添加,改进药需求迫切,年老化趋向分明。改进型新药可降低药物反作用,添加药物顺应性,对慢性病患者吸引力宏大。慢性病通常起病藏匿,病程长且病情拖延不愈,慢性病患者通常需求长工夫甚至终身服药,因而药物反作用愈加分明,同时服药依从性也是难题之一。因而降低药物反作用,进步药物顺应性的改进型新药对慢性病患者而具有弱小的吸引力。
政策端
鼓舞创新+注重临床价值为全体导向,2类新药受政策支持。新医改努力于处理我国医疗程度不高成绩,国度出台优先审批、分歧性评价、上市答应人制度等政策,对医药行业影响宏大。质量优质、临床价值高的药品受政策优惠锋芒毕露,低门槛、高反复、质量不过关的药品面临淘汰。我国医药行业将迎来企业优胜劣汰,朝向高质量和高技术的方向开展。
表2 政策鼓舞2类新药/高端制剂
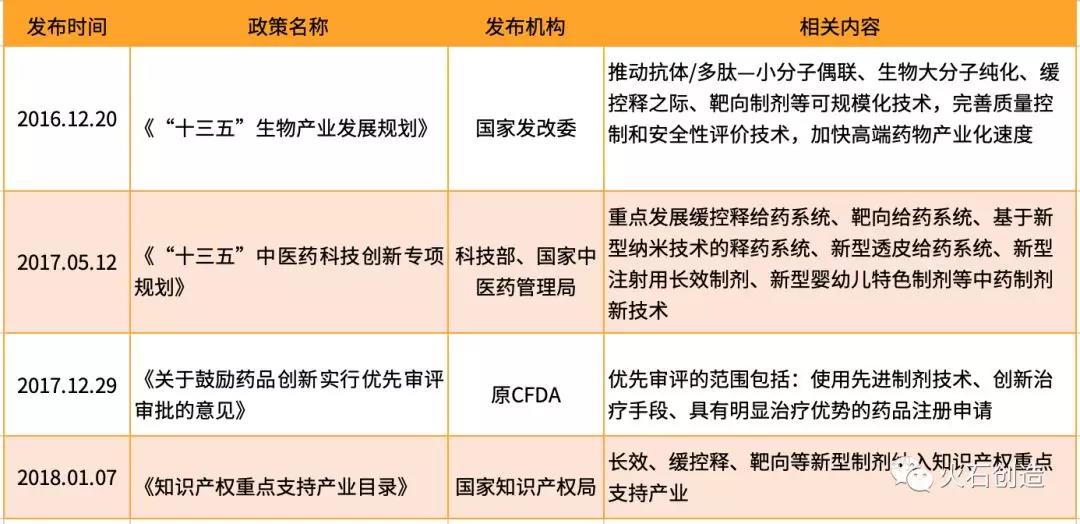
技术端
我国创新制剂技术正在奋起追逐,减少与国外差距。过来,我国制剂创新程度与国外存在较大差距。释药零碎的创新实践上离不开制剂技术、药用辅料、给药安装、制剂设备、检测设备和包装资料的创新,触及多学科,我国除了一些追踪式创新外,在制剂技术创新方面总体上相比国外程度存在较大的差距。
目前,我国创新制剂技术正在奋起追逐,创新制剂平台开端树立,多种剂型改进新药在规划中。基于我国与国际药剂研发程度的差距,近些年我国重点增强了对浸透泵、微孔膜、长效缓释、靶向、定时脉冲等国际先进剂型及相关辅料研讨。
竞争格式与趋向
制药巨头与新型制剂平台双轨并行
全球
国际制药巨头形式成熟,新型制剂平台企业近年疾速开展。
龙头企业原研产品的迭代从产品行将上市就开端规划,从而延伸公司专利药的生命周期。为了延长研发周期,寻觅最佳的给药途径,专利药企业通常采用“协作研发”的形式,即与第三类新型制剂技术型企业协作开发产品,如 Biovail、Nektar等,它们拥有抢先的技术程度,是专利药企业理想的协作同伴。
中国
涉足2类新药企业较少,规模型药企与DDS平台共求开展。
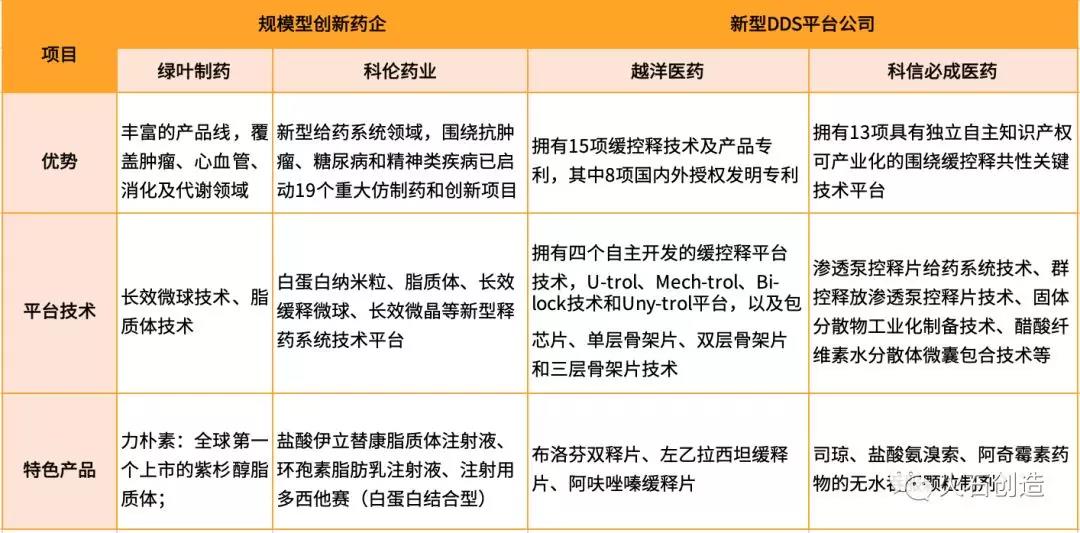
国际2类新药属于起步阶段,市场上涉足企业较少且较为分散。与美国相似,我国2类新药企业也可分为两类,一类为具有一定规模创新药企业涉足2类新药范畴,以绿叶、科伦为代表,另一类为新型药物释放零碎(DDS)平台公司,以越洋医药、科信必成等企业为代表。
表3 我国局部代表性制剂创新企业状况
总结
基于国度政策法规向创新药倾斜,在国度带量推销、仿制药分歧性评价、医保控费等医改政策高压下,仿制药利润逐年下降。同时,我国创新药研发才刚起步,可以单独开发风险性极高的“first-in-class”全球新的企业数量寥寥。但是改进型新药是在原有药物根底上停止改良,有一定临床根底,大局部产品不需求停止完好临床实验,具有本钱低、工夫短等优势。此外,改进型新药具有明显的产品特点和临床优势,在市场竞争中具有较大优势。
在《药品注册管理方法》中,改进型新药可请求打破性医治药物等在多处被提及,享用国度政策红利。在全球新药研发失败率越来越高,开发新靶点越来越难的状况下,关于无法承当创新转型的仿制药企业,改进型新药或许是一个最佳选择。乐伐替尼,
| 上一篇:mylotarg,首项100%“虚拟”临床试验启动!! | 下一篇:尼拉帕尼,第二批带量医药采购全分析!! |




